Dosages d’oxydoréduction
I. Objectifs:
* Réaliser deux dosages d'oxydoréduction.
II. Matériel:
* Une burette de Mohr de 25mL.
* Un bécher de 50mL et deux béchers de 100mL.
* Un agitateur magnétique.
* Une pipette jaugée de 20mL munie d'un pipeteur.
* Une éprouvette graduée de 10mL.
* Une solution aqueuse de permanganate de potassium de concentration Co=2,5.10-2mol.L-1.
* Une solution aqueuse de sel de Mohr de concentration Cr inconnue (environ 0,1mol.L-1).
* Une solution aqueuse d'acide sulfurique de concentration 1,0mol.L-1.
* Une pissette d'eau distillée.
* Une solution aqueuse de diiode concentration Co inconnue (environ 5,0.10-5 mol.L-1).
* Une solution aqueuse de thiosulfate de sodium de concentration Cr=1,0.10-4mol.L-1.
* Un flacon d'iodex (ou de l'empois d'amidon).
* Une spatule.
III. Dosage des ions fer (II) par les ions permanganate en milieu acide:
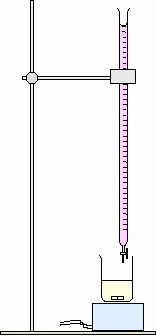
1. Montage:
Voir ci-contre.
2. Manipulation:
1. Rincer la burette à l'eau distillée, puis avec la solution aqueuse de permanganate de potassium.
2. Remplir la burette avec la solution aqueuse de permanganate de potassium.
3. Placer un volume Vr=20mL de la solution aqueuse de sel de Mohr (prélevé à l'aide de la pipette munie d'un pipeteur) dans le bécher de 50mL et y placer l'aimant de l'agitateur magnétique.
4. A l'aide de l'éprouvette graduée, ajouter avec précaution 2mL de la solution d'acide sulfurique.
5. Agiter et verser 1,0mL de la solution aqueuse de permanganate de potassium. Observer le changement de couleur.
6. Renouveler l'opération jusqu'à l'équivalence et relever le volume Vo de solution aqueuse de permanganate de potassium versé à l'équivalence.
3. Exploitation:
1. Ecrire l'équation bilan de la réaction du dosage.
2. Comment repère-t-on l'équivalence?
3. En déduire une relation entre les quantités de matière de réactif no et nr à l'équivalence.
4. En déduire la concentration Cr de la solution de sel de Mohr en ions Fe2+.